Бактерии — самые старые и самые многочисленные организмы на Земле. Кроме того, они легче всего адаптируются к условиям окружающей среды и обладают непревзойденной способностью сосуществовать с другими живыми существами, включая нас.
В нашем желудочно-кишечном тракте обитает более 1000 видов микроорганизмов (в основном бактерии, но также вирусы, простейшие, археи и грибы), которые примерно в 10 раз превышают количество клеток в организме взрослого человека. Эта коллекция микробов, известная как микробиом кишечника, эволюционировала вместе с людьми и всеми животными в течение тысяч лет, что привело к взаимовыгодным отношениям.
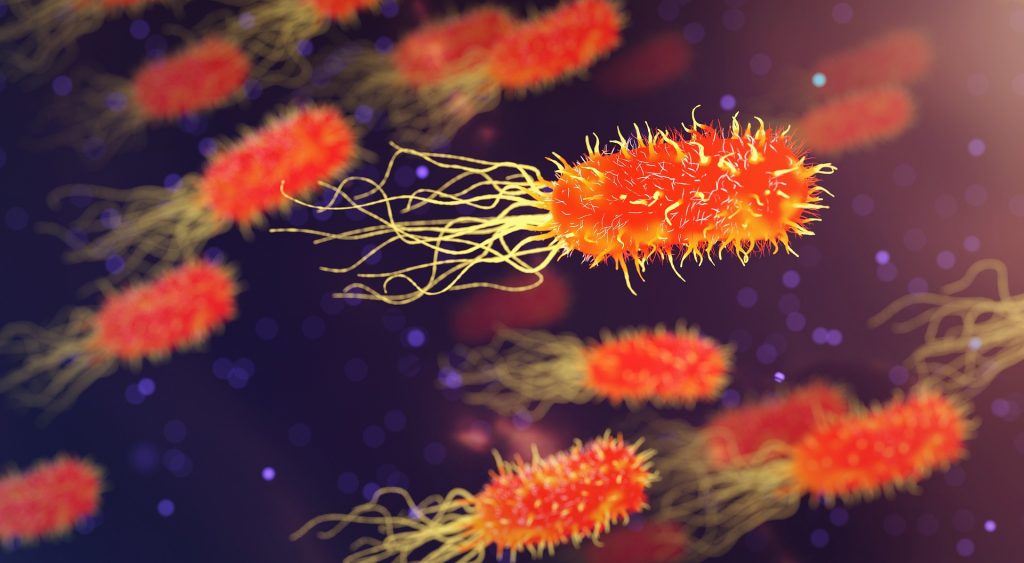
Бактериальная колонизация кишечника происходит при рождении и формируется в первые несколько лет жизни под влиянием нескольких факторов, включая роды (вагинальное или кесарево сечение), будь то кормление грудью или смесью, отлучение от груди, диета, использование антибиотиков, инфекции и стресс. Состав кишечных бактерий остается довольно постоянным у каждого из нас и, как правило, одинаков в семьях, среди близких друзей и среди людей, которые живут вместе. Однако диета, упражнения, стресс, изменения настроения, болезни и воздействие патогенов и загрязняющих веществ в окружающей среде могут влиять на баланс кишечных микробов и склонять чашу весов между болезнью и здоровьем.
Кишечные бактерии: новые лучшие друзья против боли?
Давно известно, что определенные группы кишечных бактерий чрезмерно или недостаточно представлены у людей с болезненными состояниями желудочно-кишечного тракта, такими как синдром раздраженного кишечника (СРК) и воспалительное заболевание кишечника (ВЗК). Однако только в последние несколько лет роль кишечных бактерий в регуляции боли стала горячей темой для исследований. Например, в начале этого года два отдельных исследования (рассматриваемые здесь и здесь) показали, что профили кишечного микробиома людей с широко распространенной хронической болью (фибромиалгией) отличаются от таковых у здоровых людей (включая братьев и сестер и близких родственников, побуждая к предположениям о том, могут ли определенные кишечные бактерии «удаленно» вызывать боль.
В этой серии блогов, состоящей из двух частей, мы исследуем то, что известно на данный момент о механизмах, с помощью которых изменения кишечной микробиоты могут вызывать боль в желудочно-кишечном тракте и других местах и влиять на обработку боли мозгом.

Микробиота кишечника и висцеральная боль
В настоящее время хорошо известно, что изменения в микробиоте кишечника — дисбиоз кишечника — критически влияют на развитие расстройств ЖКТ, таких как СРК, ВЗК, целиакия и пищевая аллергия. Интересно, что исследование 2017 года на мышах показало, что эти состояния не возникают внезапно, а являются результатом умеренных, повторяющихся оскорблений, которые в конечном итоге приводят к отключению защиты хозяина от воспаления. Их исследования показали, что незначительные рецидивирующие инфекции, вызванные пищевым отравлением, снижают уровень кишечной щелочной фосфатазы — фермента, который выводит токсины из LPS (эндотоксина), самого распространенного провоспалительного бактериального токсина. Это эффективно раскрывает патогенный потенциал комменсальных грамотрицательных бактерий и способствует хроническому воспалению, колиту и, в конечном итоге, ВЗК. Примечательно, что исследование показало, что повышенное провоспалительное состояние кишечной ткани сохранялось еще долго после того, как первоначальная инфекция была разрешена иммунным ответом хозяина.
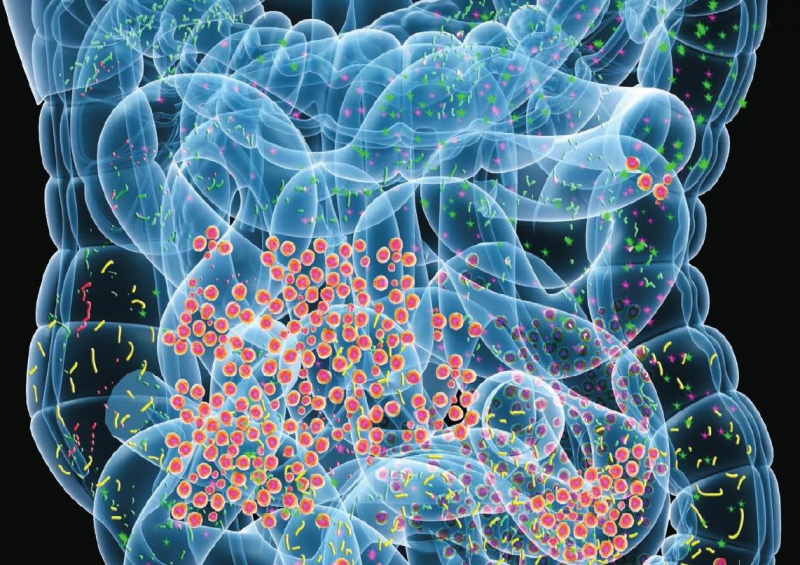
В свою очередь, исследования на животных и клинические испытания на людях подтвердили, что кишечные микробы являются важными модуляторами висцеральной боли, возникающей в результате вышеуказанных состояний. Многие сведения о свойствах и функциях кишечной микробиоты получены в результате исследований мышей, рожденных и выращенных в строгих стерильных условиях, которые предотвращают рост бактерий в любой части тела. Исследование показало, что у этих «свободных от микробов» мышей развивается висцеральная гиперчувствительность (гипералгезия), и это можно обратить вспять путем колонизации нормальной микробиотой контрольных мышей. Более того, у беспроблемных мышей наблюдались объемные изменения в областях мозга, связанные с обработкой боли (например, передняя поясная извилина коры и периакведуктальный серый цвет), которые также были обращены пополнением кишечных бактерий от мышей обычного разведения. Однако становится ясно, что природа боли также определяет влияние кишечных бактерий на восприятие боли; Чтобы проиллюстрировать этот момент, исследования показали, что мыши без микробов испытывали меньшую боль по сравнению с нормальными мышами при воздействии ЛПС, каррагинана (экстракт красных морских водорослей) или провоспалительных цитокинов.
Другие исследования, проведенные на мышах и людях, показали, что истощение кишечных бактерий антибиотиками в раннем возрасте может предрасполагать к более интенсивной и длительной висцеральной боли и расстройствам, таким как ВЗК, в более позднем возрасте, и подчеркнули преимущества пробиотиков и пребиотиков. для уменьшения симптомов. И наоборот, исследования показали, что трансплантация фекальной микробиоты от пациентов с СРК воспроизводила симптомы заболевания у крыс
Антибиотики — обоюдоострый меч
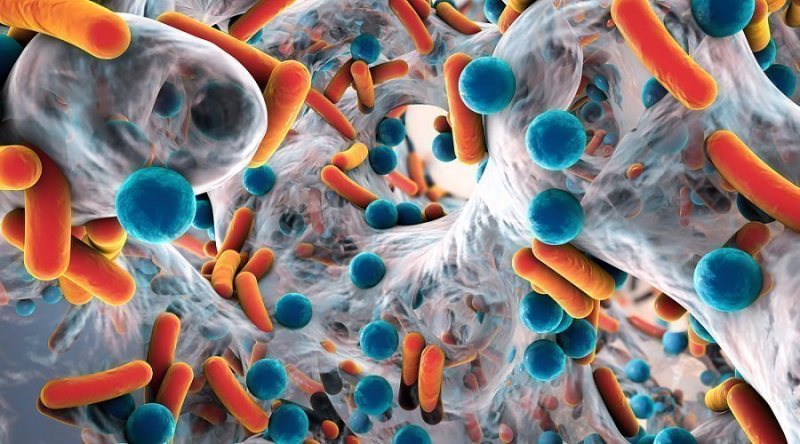
Антибиотики широкого спектра действия уничтожают не только патогенные бактерии, но и микробы, которые сбраживают бутират и другие незаменимые мелкоцепочечные жирные кислоты (SCFA), полученные из клетчатки, необходимые для поддержания микробного гомеостаза. В отсутствие бутирата метаболизм кишечника останавливается, митохондриальное бета-окисление в колоноцитах прекращается, а повышенный уровень кислорода достигает просвета желудочно-кишечного тракта. Ободочная кишка представляет собой бескислородную (анаэробную) среду, населенную доброкачественными облигатными анаэробами (в основном Firmicutes и Bacteroidetes). В присутствии кислорода патогенные факультативные анаэробы, такие как кишечная палочка, побеждают нормальные бактерии толстой кишки, что приводит к активации иммунной системы, воспалению и проявлениям заболевания желудочно-кишечного тракта (3).
Оставайтесь на связи… Во второй части этой серии блогов мы поговорим о оси кишечная микробиота-мозг и о том, как сигналы, посылаемые кишечными микробами, влияют на обработку боли в мозге.
Вы практикующий врач. Хотите узнать больше о том, как функциональное питание может изменить микробиом и облегчить хроническую боль?
Присоединяйтесь к списку ожидания программы сертификации практикующего врача по функциональному питанию при хронической боли!



Оставить комментарий